Das Virus der Afrikanischen Schweinepest (engl. African swine fever virus, ASFV) ist ein hoch ansteckender, pathogener und tödlicher Krankheitserreger der Schweine, der weltweit Haus- und Wildschweine bedroht. Zurzeit gibt es keine weitflächig zugelassenen Impfstoffe oder Behandlungen. Das Verständnis der ASFV-Biologie bezüglich der Gesamtheit der viralen Proteine (das virale Proteom), des Einflusses der Virusinfektion auf die Gesamtheit der Wirtsproteine (das zelluläre, porzine Proteom) und die Interaktion zwischen Virus und Wirt ist im Vergleich zu anderen gut-untersuchten und ähnlich komplexen Viren (z.B. Herpes- oder Adenoviren) gering. Ein besseres Verständnis der ASFV-Biologie wird zur Entwicklung von Impfstoffen und Behandlungsstrategien benötigt.
Um das Verständnis der ASFV-Biologie zu verbessern, wurden die vorangingen Zielzellen des ASFV, Schweinemakrophagen, frisch aus Schweineblut isoliert (primäre Makrophagen, siehe Abbildung 1), mit unterschiedlichen ASFV-Isolaten infiziert und Proteinproben zu unterschiedlichen Zeitpunkten der Infektionen genommen. Die Expressionsmuster von ASFV- und Wirtsproteinen wurden mittels Massenspektrometrie basierter Proteomanalyse untersucht (siehe Abbildung 2).
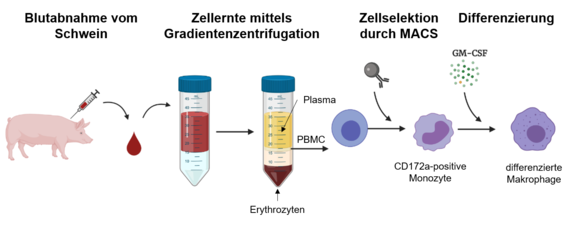
Abbildung 1: Zur Isolation von primären Schweinemakrophagen, wurde die Zellen des Blutes mittels Gradientenzentrifugation von Blutplasma und Erythrozyten getrennt. Aus den so gewonnen peripheren mononukleäre Blutzellen (engl. peripheral blood monocytic cells, PBMC) wurde durch magnetische Separation (engl. magnetic-activated cell sorting, MACS) CD172a-positive Monocyten als Vorgängerzellen selektiert. Die Reifung von CD172a-positiven Monozyten zu ausdifferenzierten Makrophagen wurde durch den Granulozyten-Makrophagen-Kolonie-stimulierende Faktor (engl. granulocyte-macrophage colony-stimulating factor, GM-CSF) induziert.
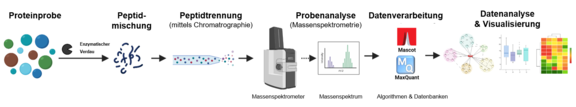
Abbildung 2: Arbeitsablauf einer Proteomanalyse mittels “Bottom-up“ Massenspektrometrie. Eine Proteinprobe wird enzymatisch zu einer Peptidmischung verdaut. Unterschiedliche Peptide werden mittels Chromatographie separiert und im Massenspektrometer analysiert. Im Anschluss an die Analyse erfolgt die Datenverarbeitung unter Einsatz verschiedener Algorithmen und Datenbanken, die qualitative und quantitative Datenanalyse und Visualisierung.
Im Rahmen meiner Dissertation konnte ich zeigen, dass das ASFV-Proteom in Makrophagen vergleichbar ist mit bereits bekannten Expressionsmustern der ASFV-Proteine aus Studien mit etablierten Zelllinien (z.B. WSL-Zellen). Die Expression von 27 ASFV-Proteinen konnte erstmals auf Proteinebene bestätigt werden. Unter ihnen 12 neue offene Leserahmen (eng. novel open reading frame, nORF), die erst kürzlich vorhergesagt wurden.
Des Weiteren konnte ich nachgewiesen, dass ASFV nicht nur die Expressionslevel von Wirtsproteinen moduliert, sondern auch die Synthese neuer Wirtsproteine kontrolliert. Neu beschriebene Einflüsse der ASFV-Infektion auf das zelluläre Proteom sind unter anderem: die veränderte Expressionsstärke von Cathepsinen, die Modulation der MAPK14/p38-Signalkaskade und der RNA-Prozessierung, sowie die erhöhte Expression von Genen der Interferonantwort (Teil der Immunreaktion), trotz einer grundsätzlich stark reduzierten Proteinsynthese.
Meine Dissertation beschreibt erstmalig das ASFV-Proteom und die Wirtsantwort auf die Infektion mit ASFV in primären Schweinemakrophagen und bietet daher neue Einblicke in die ASFV-Biologie. Diese Daten tragen dazu bei, das Verständnis der Virus-Wirt-Interaktionen zu verbessern, zeigen aber auch die Vielzahl der exprimierten ASFV-Proteine und die Komplexität ihrer Expressionsabfolge. Das derzeitige Verständnis über die Expressionsabfolge, die Funktionalität und die Interaktionen zwischen ASFV- und Wirtsproteinen bleibt lückenhaft ist und viele Aspekte der ASFV-Replikation müssen noch verstanden werden.